Saúde
Entenda o processo de aprovação da vacina da Covid-19 pela Anvisa
Em entrevista a ‘CartaCapital’, consultor da agência esmiúça aspectos políticos e técnicos para aval final a um imunizante seguro
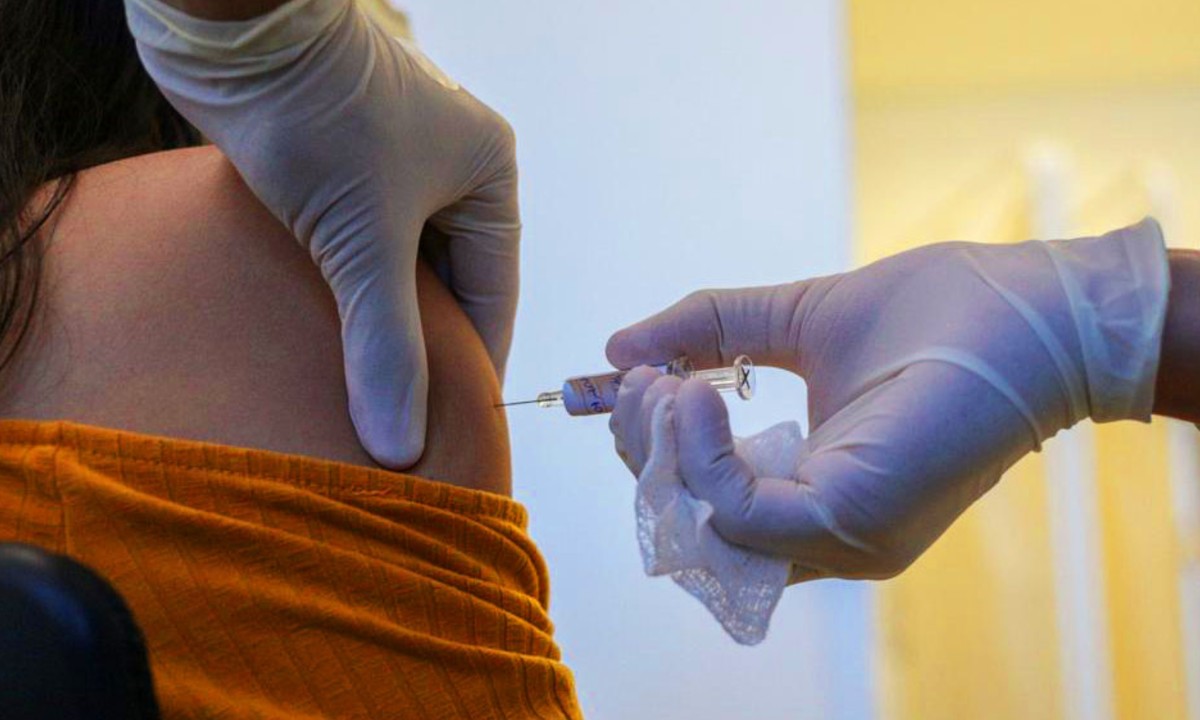
Com a divulgação de resultados clínicos das vacinas contra a Covid-19 em fase de testes, aumenta a expectativa para uma data em que os brasileiros – e o resto do mundo – poderão obter o imunizante contra o coronavírus.
Até a picada de agulha, porém, a vacina passa obrigatoriamente pela Agência Nacional de Vigilância Sanitária (Anvisa), responsável por checar a qualidade dos fármacos e dar o aval necessário de segurança para todas as faixas etárias.
Algumas informações sobre o funcionamento das vacinas ainda não foram totalmente explicadas pelos laboratórios – como a dimensão da imunização, por exemplo. Outros detalhes já dizem respeito à organização montada pelo Ministério da Saúde para garantir um programa ordenado de vacinação – desde a refrigeração adequada das doses até o treinamento dos agentes de Saúde para sua aplicação.
Quais vacinas estão em fase de testes no Brasil
 Foto: iStock
Foto: iStock
No Brasil, quatro vacinas na fase 3 – a que abrange a testagem em voluntários – tiveram estudos clínicos autorizados pela Anvisa: a de Oxford, desenvolvida também pelo laboratório Astrazeneca e pela Fiocruz; a Coronavac, da Sinovac e Instituto Butantan, a Pfizer-Wyeth e a Janssen-Cilan, da Johnson & Johnson (atualmente em pausa para estudo de efeitos adversos).
As duas primeiras estão em fase de “submissão contínua”, o que permite que a Anvisa inicie a avaliação de dados do produto e de fases já concluídas da pesquisa enquanto outros dados são gerados para compor um dossiê final, afirmou a agência em nota a CartaCapital. “Para ambos, a Anvisa já avaliou os dados submetidos e emitiu exigências às empresas para complementação de informações e dados”.
Até o momento, o Ministério da Saúde tem acordos com os dois estudos. O anúncio mais recente é de terça-feira 20, quando a pasta confirmou a compra de 46 milhões de doses da Coronavac para o SUS.
Nomeada de “vacina [contra coronavírus] mais segura do mundo” pelo diretor do Butantan, Dimas Covas, por seus bons demonstrativos relacionados aos efeitos colaterais, a Coronavac ainda precisa apresentar os resultados de eficácia em relação à geração de anticorpos. Isso só vai acontecer quando 61 voluntários forem infectados pelo coronavírus – uma fração de segurança que deve ser atingida entre novembro e dezembro, espera Covas.
A Anvisa afirma que “não existe uma eficácia mínima necessária definida por resolução da Anvisa para registro de vacinas no Brasil”, e que este ponto depende do contexto de cada doença. No caso da Covid-19, por exemplo, o órgão afirma que há um debate em torno de uma eficácia de 50%.
“O que se vem discutindo entre as autoridades reguladoras é considerar aceitável para uma vacina contra a Covid-19 uma eficácia geral de 50%, garantindo-se que a maior parte da população atinja uma eficácia mínima considerada importante para a saúde pública”, afirmam. “Ressaltamos que essa é uma discussão global e que qualquer decisão será tomada a partir do compartilhamento e conhecimento dos dados”.
Nesse cenário, é possível afirmar que uma vacina eficiente contra o coronavírus será aprovada até o fim do ano? E há riscos de influências políticas ou entraves burocráticos entrarem no meio do aval final a um fármaco seguro?
Para responder a essas questões, CartaCapital entrevistou José Cássio de Moraes, doutor em Saúde Pública e professor da Faculdade de Medicina da Santa Casa de São Paulo, que também já atuou como consultor na Anvisa para o registro de novas vacinas e é membro do comitê técnico do Sistema Nacional de Imunização, integrado ao Ministério da Saúde. Confira:
CartaCapital: Para além das discussões recorrentes sobre a eficácia das vacinas que estão em fase 3, a discussão também gira em torno do tempo útil de análise pela Anvisa até a liberação. Como funciona isso dentro da agência? Poderia dar um panorama do processo?
José Cássio de Moraes: Para uma vacina de interesse público, como no caso da Covid e de outras, a Anvisa se propõe a acompanhar principalmente a realização da fase 3. Os produtores mandam toda uma documentação para a Anvisa, justificando pelos dados das outras fases que pode ser uma vacina protetora e com certa segurança. Esse protocolo, além de ser aprovado no CONEP (Comissão Nacional de Ética em Pesquisa), também é avaliado enquanto um protocolo de pesquisa.
Com isso, [os técnicos] vão recebendo essas informações a respeito da segurança da vacina e a análise da eficácia dessa vacina – como em que faixas etárias foram feito esses estudos, a quantidade de doses, a análise da bula do medicamento. Também agendam uma visita à fábrica que produz a vacina para ver se há boas práticas de produção, se há condições de higiene e técnicas, por exemplo, ou como é feita a inativação do vírus.
No caso da Covid-19, como é uma vacina produzida em ritmo muito rápido, as agências que fazem o controle de vacinas estão estabelecendo algumas regras para poder fazer a análise. A FDA (Food and Drug Administration, agência dos Estados Unidos) já publicou um documento de 18 páginas dizendo mais ou menos o que eles vão exigir – qual o aspecto de produção, de consistência do lote. Por exemplo, quanto tempo de acompanhamento deve ter o indivíduo após ter recebido a 2ª dose? A FDA estabeleceu que no mínimo 2 meses para ver a eficácia e 1 mês para verificar eventos adversos.
Que eu saiba, a Anvisa não colocou ou deu publicidade a que pontos ela vai abordar. Então a gente ainda não conhece. Normalmente, as análises da Anvisa faz são sérias e adequadas, e o que a gente espera agora é que não tenha nenhuma influência política nessa análise.
CartaCapital: Quais seriam as consequências de uma “influência política”? O que você quer dizer com isso?
José Cássio de Moraes: A Anvisa faz parte de uma comissão internacional de avaliação de produtos. Um produto avaliado pela Anvisa tem facilidade de ser aceito pela FDA, EMA e vice e versa, porque já tem o aval de uma agência regulatória que cumpre todos os requisitos.
Se [uma agência] fizer um tipo de avaliação não correta, com influência política, isso compromete a acreditação que a Anvisa tem hoje no cenário internacional a respeito da avaliação de produtos.
A Anvisa é formada por cinco diretores com mandato. Foram aprovados recentemente três diretores pelo Senado após serem indicados pelo presidente. Eles têm mandato fixo. Quanto muda de presidente, não pode simplesmente tirar as pessoas que fazem parte dessa diretoria.
O importante seria que a Anvisa declarasse os critérios para análise. Um exemplo é o que acontece na FDA: a reunião que faz a avaliação e o julgamento final de um produto é aberta. As pessoas não têm direito a voto, mas de ouvir o que as pessoas estão falando. O que é segredo de produção não é aberto, mas os resultados clínicos e de segurança sim. Tem um parecer, e esse parecer é analisado e aprovado, e é uma discussão aberta. Qualquer pessoa pode se inscrever e, se quiser, pode encaminhar perguntas.
A Anvisa não tem isso, mas tem que escrever muito bem uma justificativa do porquê da aceitação ou não, e tem que ter um cronograma de casos. Ou seja, após receber todos os produtos, em 30 dias ou 60 dias, eu dou um parecer para não ficar empurrando com a barriga ou exigir documentos a mais. Senão para enrolar é fácil. Pede um documento, pede outro, e cai na burocracia fácil.
CartaCapital: Tem algum histórico disso ter acontecido?
José Cássio de Moraes: Na área de vacina, que a gente acompanha mais de perto, não. Nunca soube que houve essa situação de empurrar a decisão. As empresas [farmacêuticas] já conhecem essas exigências e têm funcionários especializados nessa questão da agência regulatória. Normalmente, elas já apresentam toda a documentação.
Isso dá uma validação das decisões que a Anvisa toma e gera mais segurança para a população, mais confiança. É um patrimônio que não se pode perder porque, se perder, é muito difícil recuperá-lo depois.
 Broche em funcionário da Anvisa. Foto: Fernando Frazão/Agência Brasil
Broche em funcionário da Anvisa. Foto: Fernando Frazão/Agência Brasil
CartaCapital: No dia 30 de setembro, o gerente-geral de medicamentos e produtos biológicos da Anvisa, Gustavo Mendes Lima Santos, falou que a agência pode flexibilizar os critérios de eficácia para aprovação de uma vacina contra a Covid-19 com 50% de eficácia mínima em vez de 70%. Você acha que esse é um caminho plausível?
José Cássio de Moraes: Isso é separado em dois aspectos: um é para você impedir a transmissão e outro é para evitar casos graves.
A vacina da gripe previne 20 a 30% a infecção das pessoas pelo vírus da gripe, mas tem uma proteção maior contra as formas graves. O objetivo da vacina seria não impedir a transmissão, mas impedir formas graves – esse é o objetivo da vacina da influenza ou do rotavírus humano aplicado em crianças.
As vacinas em teste certamente não estarão prontas até o final deste ano. Em 2020, acho que não será aplicada nenhuma dose de vacina em qualquer grupo
Outras vacinas tem o papel de eliminar a transmissão. Quando você toma a vacina do sarampo, não vai transmitir mais o sarampo para outras pessoas, por exemplo. Tem que se analisar ao que a vacina se propõe. Para isso existem as exigências para verificar se ela elimina a transmissão ou se ela evita um caso grave. E sempre depende da força de transmissão.
Uma vacina de sarampo, com 70% [de eficácia mínima] é insatisfatório, porque para cada caso de sarampo, uma pessoa infectada transmite para 18 pessoas. Na Covid, não há essa transmissão para 18 pessoas – o máximo que se conseguiu foi 1 para 4, então pode ter uma eficácia menor. Depende um pouco dessa capacidade de transmissão que tem o agente. Se é uma forma grave, por exemplo, como a gripe, a eficácia de 60% para evitar forma grave já é um dado importante principalmente em gestantes, pessoas com comorbidades, idosos. Tudo isso depende do objetivo da vacina.
É preciso se perguntar: o que você pretende com essa vacina? Aí você pode analisar se esse objetivo foi cumprido ou não, se foi um estudo bem feito, se a avaliação do desfecho final que você pretende foi bem medido. Se o desfecho final é evitar a transmissão, você tem que comprovar isso. Se é evitar casos graves, também.
Sobre a Coronavac, por exemplo, esses objetivos ainda não foram publicizados. Mas o mais provável é que vai ser para evitar casos graves porque a análise de transmissão é mais complicada. É uma análise que demora mais tempo para ser feita.
As vacinas em teste certamente não estarão prontas até o final deste ano. Em 2020, acho que não vai ser aplicada nenhuma dose de vacina em qualquer grupo que seja.
CartaCapital: A Anvisa também faz parte da estratégia de distribuição de vacinas ao redor do País? Se houver um acordo de produção nacional de uma vacina, por exemplo, qual é a estrutura mobilizada dentro do ministério?
José Cássio de Moraes: A Anvisa participava da comissão de imunização, e, depois que a vacina é liberada, parte para um comitê do Ministério da Saúde, o CONITEC. Depois, passa para o Programa Nacional de Imunização, que vai definir os grupos alvos, quando vai começar, qual estratégia será feita.
É um programa complicado, porque [para a Covid] são duas doses, e geralmente vacina de campanha é de uma dose só. Tem que aproveitar a rede de distribuição que já existe para as outras vacinas, comprar seringa e agulha, treinar as pessoas para aplicação, ter vigilância dos eventos adversos – a chamada fase 4 da doença, que é analisar os impactos da vacina.
Serão necessárias cerca de 500 milhões de doses para imunizar todo mundo. Não vai ter essa produção [rápida] nunca, nenhum laboratório tem condições disso. Não se produz uma vacina do mesmo jeito que uma aspirina
A gente tem essa tradição. Nós temos o programa mais amplo do mundo. A única vacina não incluída no Plano Nacional de Imunização é a vacina da meningite-B. Todos os demais, o setor privado ou público, tem acesso a todas as vacinas.
Tem que ter um planejamento muito bom para evitar invasão de centro de saúde, e o ideal é que se tenha uma política nacional . Se vacinar São Paulo e não o resto do Brasil, por exemplo, vai ter invasão no estado de SP pra ter vacina, e a perda do caráter do PNI, que é universal, descentralizado, equitativo.
Serão necessárias cerca de 500 milhões de doses para imunizar todo mundo. Não vai ter essa produção [rápida] nunca, nenhum laboratório tem condições disso. Não se produz uma vacina do mesmo jeito que uma aspirina.
CartaCapital: Você se sente positivo sobre a execução correta de todas essas fases?
José Cássio de Moraes: A gente tem uma experiência em fazer essas campanhas. Essa tem uma dificuldade maior porque são duas doses. Já tem uma rede de frios – para a conservação da vacina -, 36 mil postos de vacinação, cada posto tem sua geladeira, existe uma estrutura de logística que permite a distribuição e conservação.
Lógico que tem dificuldade porque você tem uma redução de pessoas que trabalham no setor de saúde, isso faz com que a agilidade seja menor porque você tem uma queda de investimento no SUS. Parece que o SUS foi redescoberto esse ano por algumas pessoas.
Precisa ser muito bem planejado, e a população precisa ser informada sobre quando será vacinada, senão será um salve-se quem puder. Precisa ser [uma campanha] muito bem planejada e com uma boa estratégia de comunicação para convencer cada cidadão que estará incluído nessa ou naquela fase. A gente sabe que todo mundo tem a ansiedade de ser vacinado o quanto antes for possível, mas é inviável – não tem como vacinar 100 milhões de pessoas simultaneamente no País.
CartaCapital: Por mais que a vacina seja uma notícia muito esperada, ela não dá conta de resolver toda a situação. Na sua avaliação, o Brasil corre o risco de sofrer com uma ‘segunda onda’? Devemos ser afetados pela alta de casos na Europa e, ao mesmo tempo, a situação de grande flexibilização em diversos estados?
José Cássio de Moraes: Tudo indica que a vacinação não é a bala de prata. As hipóteses mais prováveis é que ela vai evitar casos graves – já é a esperança maior de todos nós, que é evitar o óbito. A gente não tem informações que ela vai evitar a transmissão.
Com isso, a gente precisa manter estratégias para atender e acompanhar a pandemia. As coisas não foram muito bem feitas aqui. A única coisa que a gente teve foi uma reorganização do SUS no atendimento dos casos mais graves, e em alguns estados aconteceu das pessoas ficarem dias para serem internadas.
O SUS precisa ser valorizado, e ele está em deterioração, com menos verba. Ele tem que ser reativado, sair da UTI para oferecer um atendimento melhor para a população, porque ele demonstrou sua importância
Todas as outras coisas que os outros países fizeram a gente não fez. A gente teve um distanciamento social meia boca. Em São Paulo, o máximo foi 50 ou 60%, e hoje você vê gente andando por aí sem usar máscara. A medida que a gente vai relaxando, a gente pode retornar a um aumento da prevalência da doença.
Na Europa, você teve uma fase, depois caiu bastante e agora está voltando de novo. É uma doença que tem chances de se manter, mas você pode minimizar e melhorar o controle dela adotando medidas mais adequadas, com uma política nem de minimização dos riscos e nem de maximização deles. Nós não tivemos uma organização boa para enfrentar essa pandemia.
Nós vimos a importância de ter o SUS. Imagina se não tivéssemos o SUS e as pessoas tivessem que pagar para ser atendidas? O SUS precisa ser valorizado, e ele está em deterioração, com menos verba, em crise já há muito tempo. Ele tem que ser reativado, reanimado, sair da sua UTI para oferecer um atendimento melhor para a população porque ele demonstrou sua importância.
A gente não saiu ainda da 1ª onda, a gente pode ter quedas, mas está num patamar elevado. 500 óbitos por dia não é um patamar bom. Por mais que antes a gente tivesse 1.000, mas mesmo 500 óbitos por dia é elevado. A gente precisa ver se essa queda é consistente, se vai permanecer por várias semanas.
Antes, em média, por óbito, você tinha 3.600 óbitos por dia por todas as causas. Hoje se tem 500 só de uma causa. Ainda é um patamar elevado. 25 mil casos diários – isso com toda a pobreza de testagem que a gente tem, porque uma parte desse aumento da Europa foi devido a se organizar mais a questão da testagem.
Apoie o jornalismo que chama as coisas pelo nome
Os Brasis divididos pelo bolsonarismo vivem, pensam e se informam em universos paralelos. A vitória de Lula nos dá, finalmente, perspectivas de retomada da vida em um país minimamente normal. Essa reconstrução, porém, será difícil e demorada. E seu apoio, leitor, é ainda mais fundamental.
Portanto, se você é daqueles brasileiros que ainda valorizam e acreditam no bom jornalismo, ajude CartaCapital a seguir lutando. Contribua com o quanto puder.