CartaExpressa
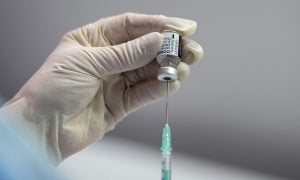
Anvisa autoriza testes da Butanvac com voluntários
Serão aplicadas duas doses, com um intervalo de 28 dias, esclareceu a agência nesta quarta-feira 9


A Agência Nacional de Vigilância Sanitária concedeu autorização, nesta quarta-feira 9, para a pesquisa clínica da vacina contra a Covid-19 do Instituto Butantan, a Butanvac. O imunizante será aplicado em humanos pela primeira vez, dando início aos testes de fase 1 e 2 da pesquisa clínica.
Ao todo, as fases 1 e 2 devem contemplar mais de 6 mil voluntários com 18 anos ou mais; mas, neste momento, está autorizada a fase A do estudo, com 400 voluntários.
Serão aplicadas duas doses, com um intervalo de 28 dias, esclareceu a Anvisa. O estudo deve ser realizado no Hospital das Clínicas e no Hospital das Clínicas da Faculdade de Medicina de Ribeirão Preto.
A Butanvac é a primeira vacina contra a Covid-19 produzida no Brasil e que não depende da importação de matéria-prima. A expectativa é de que um total de 18 milhões de doses esteja pronto ainda neste mês, e mais 40 milhões até o fim do ano.
2026 já começou
Às vésperas das eleições de 2026, o País volta a encarar um ponto de inflexão: o futuro democrático está novamente em jogo.
A ameaça bolsonarista não foi derrotada, apenas recuou. No Congresso, forças conservadoras seguem ditando o ritmo. Lá fora, o avanço da extrema-direita e os conflitos em Gaza, no Irã e na Ucrânia agravam a instabilidade global.
Se você valoriza o jornalismo crítico, independente e comprometido com a democracia, este é o momento de agir.
Assine ou contribua com o quanto puder.