Saúde
Anvisa autoriza uso emergencial de vacinas da Covid-19
Voto da relatora foi acompanhado por todos os diretores. Medida é temporária e não deve ser igualado ao processo de registro da vacina
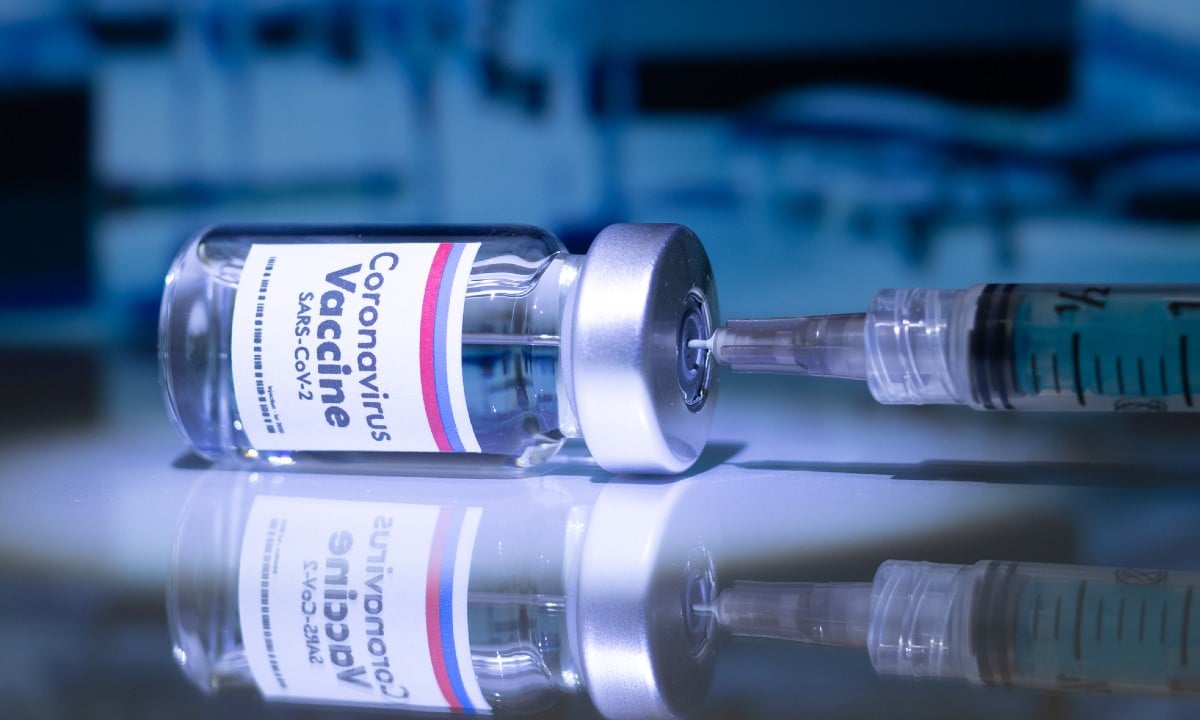
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, nesta quinta-feira 10, uma autorização para o uso emergencial de vacinas para a Covid-19.
A autorização das resoluções não substitui o processo de registro das diferentes vacinas do mercado na Agência.
A relatora do processo, Alessandra Bastos Soares, afirmou em voto que a “a ação da Anvisa na definição da resposta emergencial precisa continuar ocorrendo de forma ágil e proporcional ao cenário da pandemia, no intuito de de mitigar os efeitos diretos e indiretos da doença”. Ela foi acompanhada por todos os outros diretores da Agência.
Destaca-se ainda que a autorização é emergencial e temporária, e que o pedido deverá ser feito diretamente pela empresa fabricante da vacina junto a Anvisa. Até o momento, nenhum pedido foi registrado.
Apoie o jornalismo que chama as coisas pelo nome
Muita gente esqueceu o que escreveu, disse ou defendeu. Nós não. O compromisso de CartaCapital com os princípios do bom jornalismo permanece o mesmo.
O combate à desigualdade nos importa. A denúncia das injustiças importa. Importa uma democracia digna do nome. Importa o apego à verdade factual e a honestidade.
Estamos aqui, há mais de 30 anos, porque nos importamos. Como nossos fiéis leitores, CartaCapital segue atenta.
Se o bom jornalismo também importa para você, nos ajude a seguir lutando. Assine a edição semanal de CartaCapital ou contribua com o quanto puder.



