Saúde
Governo pretende importar 10 milhões de doses da Sputnik V, mas quer preço ‘competitivo’
A intenção foi transmitida pelo secretário-executivo Élcio Franco ao laboratório União Química, que produzirá o imunizante no Brasil
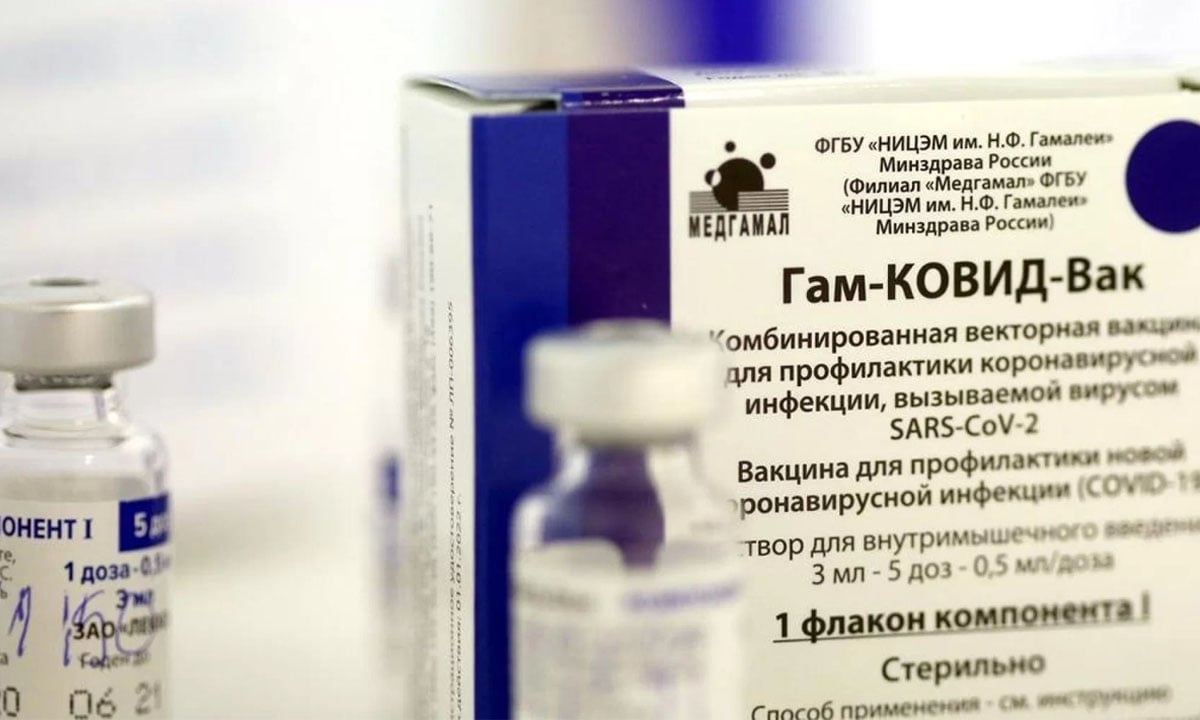
O Ministério da Saúde anunciou nesta sexta-feira 5 que pode importar dez milhões de doses da vacina russa Sputnik V, a depender de autorização da Agência Nacional de Vigilância Sanitária e de um preço “competitivo”.
A informação foi transmitida pelo secretário-executivo da pasta, Élcio Franco, a representantes do laboratório União Química, que produzirá o imunizante no Brasil. Na quinta-feira 4, o Senado aprovou uma medida provisória que abre caminho para a compra da vacina russa.
Pelo texto, a Anvisa passa a ter o prazo de cinco dias para autorizar o uso emergencial de imunizantes contra a Covid-19 que já tenham recebido aval de agências reguladoras internacionais. A MP ainda precisa ser sancionada pelo presidente Jair Bolsonaro.
Para obter autorização de uso emergencial em cinco dias, o imunizante deve ter sido aprovado em pelo menos uma das agências reguladoras internacionais listadas: as agências dos Estados Unidos, da União Europeia, do Japão, da China, do Canadá, do Reino Unido, da Coreia, da Rússia e da Argentina.
“Iremos contratar e comprar as dez milhões de doses se o preço for plausível, e efetuaremos o pagamento após a Anvisa dar a autorização para uso emergencial da Sputnik V, fazendo a disponibilização imediatamente aos brasileiros”, disse Élcio Franco.
Na quarta-feira, 3, o Ministério da Saúde afirmou que negocia a compra de 30 milhões de doses da vacina de Oxford e da indiana Covaxin, fabricada pelo laboratório Bharat Biotech. O anúncio foi feito na mesma data em que a Anvisa anunciou a retirada de algumas exigências para que os imunizantes possam ser aplicados no País, como a necessidade de realização de testes da fase três em território nacional.
Em nota, a Anvisa informou que “quando a vacina Covid-19 não estiver sendo avaliada em ensaios clínicos conduzidos no Brasil, caberá à requerente apresentar a estratégia do patrocinador quanto à condução dos estudos clínicos, demonstrando a intenção de acompanhamento dos participantes para a avaliação de eficácia e segurança dos participantes do estudo pivotal por pelo menos 1 ano, incluindo estratégia para avaliação de exacerbação da doença respiratória (RDE), e garantir que terá acesso aos dados gerados em sua totalidade, bem como demonstrar que os estudos pré clínicos e clínicos foram conduzidos conforme as diretrizes aceitas nacional e internacionalmente”.
Apoie o jornalismo que chama as coisas pelo nome
Os Brasis divididos pelo bolsonarismo vivem, pensam e se informam em universos paralelos. A vitória de Lula nos dá, finalmente, perspectivas de retomada da vida em um país minimamente normal. Essa reconstrução, porém, será difícil e demorada. E seu apoio, leitor, é ainda mais fundamental.
Portanto, se você é daqueles brasileiros que ainda valorizam e acreditam no bom jornalismo, ajude CartaCapital a seguir lutando. Contribua com o quanto puder.